토파시티닙 구연산염은 원래 화이자에서 경구용 JAK(야누스 키나제) 억제제 계열을 위해 개발한 처방약(상품명 Xeljanz)입니다. 이는 JAK 키나제를 선택적으로 억제하고 JAK/STAT 경로를 차단하여 류마티스 관절염, 건선 관절염, 궤양성 대장염 및 기타 면역 질환을 치료하는 데 사용되는 세포 신호 전달 및 관련 유전자 발현 및 활성화를 억제할 수 있습니다.
이 약물에는 정제, 서방형 정제 및 경구 용액의 세 가지 제형이 포함됩니다. 정제는 2012년 FDA의 첫 승인을 받았으며, 서방형 제형은 2016년 2월 FDA의 승인을 받았습니다. 류마티스 관절을 치료하는 최초의 제품입니다. Yan은 하루에 한 번 경구 복용하는 JAK 억제제입니다. 2019년 12월, 중등도~중증 활동성 궤양성 대장염(UC)에 대한 서방형 약물의 새로운 적응증이 다시 승인되었습니다. 또한, 현재 판상 건선에 대한 3상 임상시험이 완료되었으며, 활동성 건선성 관절염, 소아 특발성 관절염 등을 대상으로 6개의 3상 임상시험이 진행 중입니다. 1일 1회 복용하면 지속시간이 긴 서방정의 장점은 환자의 질병 관리 및 조절에 도움이 된다.
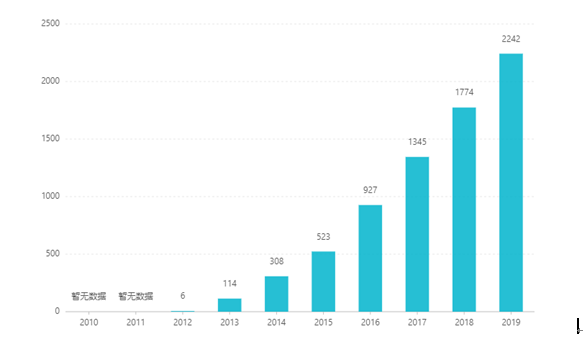
상장 이후 매출액은 해마다 증가해 2019년에는 22억4200만 달러에 달했다. 중국에서는 2017년 3월 정제 제형의 시판 승인을 받았고, 2019년 협상을 통해 의료보험 카테고리 B 카탈로그에 진입했다. 입찰가는 RMB 26.79입니다. 그러나 서방성 제제의 높은 기술적 장벽으로 인해 이 제형은 아직 중국에서 시판되지 않고 있다.
JAK 키나제는 염증에서 중요한 역할을 하며, 그 억제제는 특정 염증성 질환과 자가면역 질환을 치료하는 것으로 나타났습니다. 현재까지 전 세계적으로 승인된 JAK 억제제는 레오파마의 델고시티닙, 세엘진의 페드라티닙, 애브비의 우파티닙, 아스텔라스의 페피티닙, 엘리릴리의 바리티닙, 노바티스의 로코티닙 등 7개다. 그러나 위에서 언급한 약물 중 중국에서는 토파시티닙, 바리티닙, 로코티닙만 승인되었습니다. 치루의 '토파팁 구연산염 서방정'이 조속히 승인돼 더 많은 환자들에게 혜택을 주기를 기대한다.
중국에서는 원래 연구용 토파시티브 구연산염이 2017년 3월 NMPA의 승인을 받아 메토트렉세이트에 대한 효능이 불충분하거나 불내성이 있는 성인 RA 환자의 치료에 Shangjie라는 상품명으로 승인되었습니다. 마이네넷(Meinenet) 자료에 따르면 2018년 중국 공공 의료기관의 토파시티브 구연산염 정제 매출은 834만 위안으로 글로벌 매출보다 훨씬 낮았다. 이유의 큰 부분은 가격입니다. 상지에의 초기 소매가격은 2085위안(5mg*28정), 월 사용료는 4170위안으로 일반 가정에 적지 않은 부담이 되는 것으로 알려졌다.
하지만 토파시티브가 2019년 11월 협상을 거쳐 2019년 국민의료보험청의 '국민기본의료보험, 산재보험, 산모보험 약품 목록'에 포함된 것은 축하할 만하다. 월 사용료가 인하될 것으로 전해진다. 가격 인하 협상 후 2,000위안 이하로 낮추어 약품의 가용성을 크게 향상시킬 것입니다.
2018년 8월, 국가지식재산청 특허재심사위원회는 심사결정 제36902호 무효심판청구를 하였고, 명세서 공개가 불충분하다는 이유로 복합특허인 화이자토파티브의 핵심특허를 무효로 선언하였다. 그러나 화이자토파티브 결정형 특허(ZL02823587.8, CN1325498C, 출원일 2002.11.25)는 2022년 만료된다.
Insight 데이터베이스에 따르면 독창적인 연구 외에도 Chia Tai Tianqing, Qilu, Kelun, Yangtze River 및 Nanjing Chia Tai Tianqing의 5개 제네릭 의약품이 국내 토파시티닙 정제 제제에 대한 판매 승인을 받은 것으로 나타났습니다. 하지만 서방정형의 경우 지난 5월 26일 원연구사인 화이자만이 판매허가신청서를 제출했다. 이 제제에 대한 판매신청서를 제출한 국내 업체는 치루가 처음이다. 또한 CSPC Ouyi는 BE 시험 단계에 있습니다.
Changzhou Pharmaceutical Factory(CPF)는 중국 장쑤성 창저우에 위치한 완제 API 의약품 제조업체입니다. CPF는 1949년에 설립되었습니다. 우리는 2013년부터 Tofacitinib Citrate에 전념했으며 이미 DMF를 제출했습니다. 우리는 여러 국가에 등록했으며 Tofacitinib Citrate에 대한 최고의 문서 지원으로 귀하를 지원할 수 있습니다.
게시 시간: 2021년 7월 23일